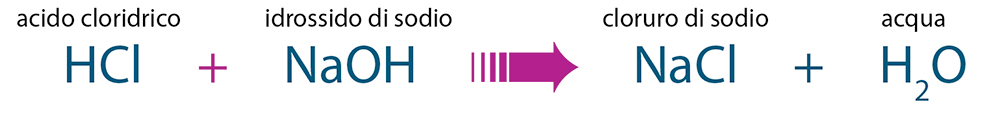
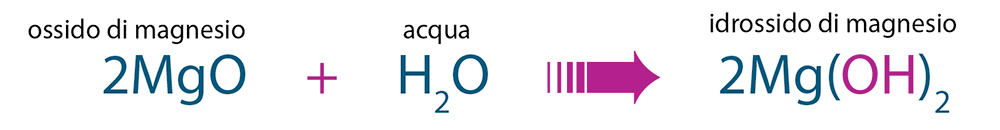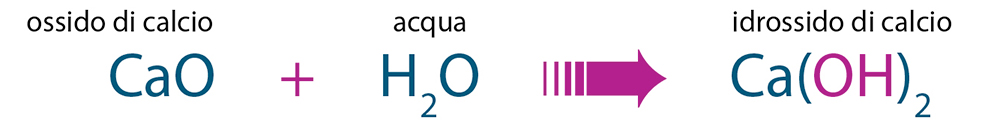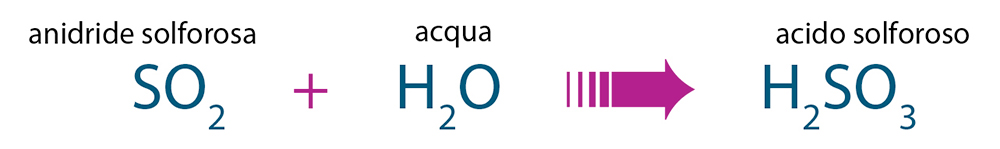SCIENZE + Proprietà di alcuni acidi, basi e sali
Molti dei liquidi con cui abbiamo a che fare quotidianamente sono acidi, per esempio il
succo di limone o l’aceto. Gli acidi possono intaccare sostanze solide anche molto dure e compatte, come i metalli o il marmo: gocce di limone, infatti, “macchiano” in modo indelebile il marmo rendendolo opaco. Questa proprietà è utilizzata in molti processi produttivi, per esempio nell’estrazione dei metalli. Sono acidi anche i succhi gastrici presenti nel nostro stomaco; essi infatti partecipano alla digestione “attaccando” i cibi ingeriti.
Anche le basi ci sono piuttosto familiari: sono basi l’ammoniaca, utilizzata tra l’altro per fare le pulizie, e la soda caustica, con cui si liberano le tubature idrauliche incrostate. Le sostanze molto basiche sono aggressive e intaccano, per esempio, i metalli, ma anche i grassi e i tessuti che costituiscono il nostro organismo. Per questa ragione gli sgrassatori universali vanno maneggiati con molta attenzione: possono “bruciare” la pelle.
La parola sale ci fa pensare al sale da cucina, ma sono sali anche la candeggina (o ipoclorito di sodio), il carbonato di calcio che forma le incrostazioni calcaree, le stalattiti e le stalagmiti, le conchiglie dei molluschi e il bicarbonato di sodio che si usa come digestivo. Un sale si distingue perché presenta sempre un legame tra un metallo e un non metallo. Di solito, inoltre, i sali a temperatura ambiente sono allo stato solido e formano cristalli che si possono osservare a occhio nudo.