la tavola periodica degli elementi
La tavola periodica, ideata nell’Ottocento dal chimico russo Dmitrij Mendeleev, è uno schema nel quale sono riportati tutti gli elementi finora conosciuti (118 in tutto; alcuni sono presenti in natura, altri sono stati creati in laboratorio).
L’ordine di disposizione degli elementi non è casuale, ma fornisce molte informazioni su di essi.
Nella tavola periodica gli elementi sono disposti in successione per valori crescenti di Z, ossia al crescere del numero di protoni presenti nel nucleo. Ogni elemento è inserito in una casella e contrassegnato, oltre che dal suo simbolo e dal suo nome, anche dal numero atomico.
Nella tavola periodica gli elementi sono ordinati lungo periodi (righe) e gruppi (colonne). Lungo ciascun periodo gli elettroni di valenza aumentano gradualmente, uno per volta. Ogni gruppo riunisce elementi con proprietà chimiche simili, vista l’analoga distribuzione degli elettroni nei loro orbitali di valenza.
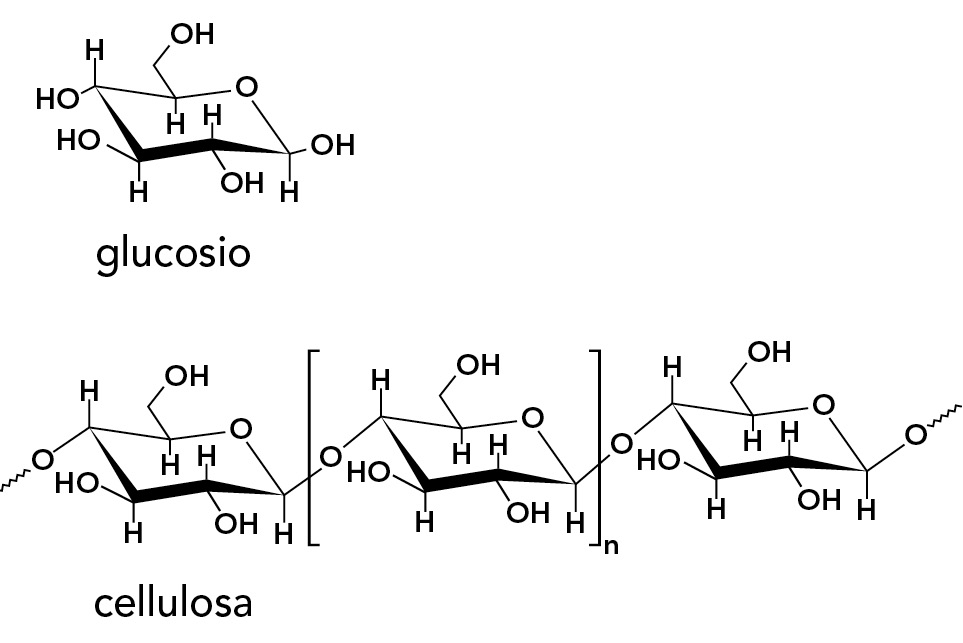
Nella tavola degli elementi si può seguire l’andamento di un’importante proprietà della materia: l’elettronegatività (EN). Essa rappresenta il potere di attrazione di un atomo nei confronti degli elettroni del legame con un altro atomo.
Nella tavola periodica, l’elettronegatività aumenta da sinistra verso destra e dal basso verso l’alto. In base alla loro elettronegatività gli elementi possono essere distinti in metalli e non metalli.
- I metalli si trovano nei primi gruppi, con bassa elettronegatività; hanno una propensione maggiore a cedere i propri elettroni e dunque a trasformarsi in ioni positivi (cationi). Hanno l’aspetto di solidi lucidi (tranne il mercurio, che è liquido) e sono buoni conduttori di calore e di corrente elettrica, oltre che facilmente lavorabili (malleabili).
- I non metalli occupano i gruppi più a destra, con alta elettronegatività, e tendono ad acquistare elettroni, diventando così ioni negativi (anioni). A temperatura ambiente si presentano in tutti e tre gli stati di aggregazione, sono opachi, pessimi conduttori di calore e di corrente elettrica.
Gli atomi con caratteristiche intermedie sono invece detti semimetalli.
Gli elementi dell’ultimo gruppo sono detti gas nobili e molto difficilmente si combinano con altri elementi.